研究概要
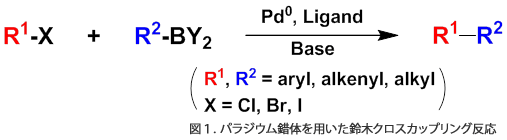 もの創りはサイエンスすべての基本であり,我々化学者は,その時々の社会の要請に応えることができるよう,日々精進しております。2010年のノーベル化学賞は,リチャード・ヘック先生,根岸先生,鈴木先生が受賞され,そのタイトルは「有機合成におけるパラジウム触媒クロスカップリング」でした。その例として,鈴木カップリング反応を図1に示しました。この反応は医薬品や電子材料など様々な化学物質の効率的合成を可能とするものです。錯体触媒では,パラジウムだけでなく,周期表で同じ周期に属するルテニウムやロジウムなども,中心金属として用いられます。ノーベル化学賞において,わざわざ枕詞としてパラジウムをつけているのは,その触媒活性が極めて高いためです。
もの創りはサイエンスすべての基本であり,我々化学者は,その時々の社会の要請に応えることができるよう,日々精進しております。2010年のノーベル化学賞は,リチャード・ヘック先生,根岸先生,鈴木先生が受賞され,そのタイトルは「有機合成におけるパラジウム触媒クロスカップリング」でした。その例として,鈴木カップリング反応を図1に示しました。この反応は医薬品や電子材料など様々な化学物質の効率的合成を可能とするものです。錯体触媒では,パラジウムだけでなく,周期表で同じ周期に属するルテニウムやロジウムなども,中心金属として用いられます。ノーベル化学賞において,わざわざ枕詞としてパラジウムをつけているのは,その触媒活性が極めて高いためです。
一方,我が国発の施策として,「元素戦略」というものがあります。元素戦略とは,「元素」の個性に焦点を当てて,新たな物質材料化学の基盤を築こうとするものです。資源の乏しい我が国の現状を考えると,パラジウムなど希少な金属ではなく,できるだけありふれた金属で,これまでに無い新機能の探索を行っていく必要があります。
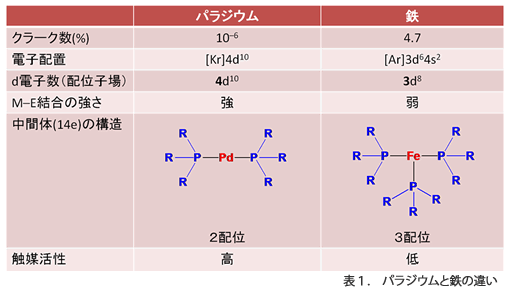 表1にパラジウムと鉄の元素の個性をまとめました。クラーク数は地球上の我々人間が活動する領域での元素の存在率を示したもので,鉄の方が断然多く存在することが分かります。また,周期表では鉄は8族,パラジウムは10族に位置し,周期でいうと鉄は第3周期,パラジウムは第4周期にあります。これらの性質を反映して,酸化数0を仮定すると錯体中では鉄は3d8の電子配置をとり,パラジウムは4d10の電子配置をとることになります。この電子配置の違いが触媒活性にも反映されていると考えられます。つまり,主量子数が1つ大きいd軌道をもつパラジウムの方が様々な元素と安定な結合を形成します。また,触媒反応において活性種となる14電子錯体を形成する際に,パラジウムは2配位となるのに対し,鉄は3配位となります。当然のことながら,2配位の方が金属中心が立体的に空いており,反応性が高くなります。以上の考察からも,鉄よりもパラジウムの方が触媒活性が高く,これまで魔法の金属として頻繁に用いられてきたことが理解できます。
表1にパラジウムと鉄の元素の個性をまとめました。クラーク数は地球上の我々人間が活動する領域での元素の存在率を示したもので,鉄の方が断然多く存在することが分かります。また,周期表では鉄は8族,パラジウムは10族に位置し,周期でいうと鉄は第3周期,パラジウムは第4周期にあります。これらの性質を反映して,酸化数0を仮定すると錯体中では鉄は3d8の電子配置をとり,パラジウムは4d10の電子配置をとることになります。この電子配置の違いが触媒活性にも反映されていると考えられます。つまり,主量子数が1つ大きいd軌道をもつパラジウムの方が様々な元素と安定な結合を形成します。また,触媒反応において活性種となる14電子錯体を形成する際に,パラジウムは2配位となるのに対し,鉄は3配位となります。当然のことながら,2配位の方が金属中心が立体的に空いており,反応性が高くなります。以上の考察からも,鉄よりもパラジウムの方が触媒活性が高く,これまで魔法の金属として頻繁に用いられてきたことが理解できます。
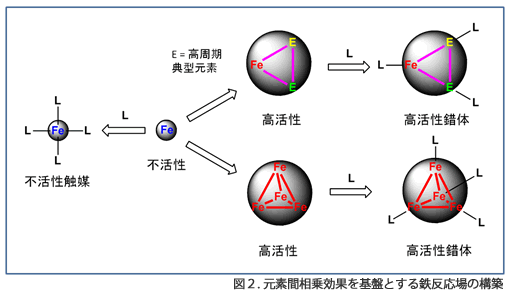
このように鉄よりもパラジウムの方が触媒活性が高いのは明らかであり,鉄を触媒として用いるためには,ブレイクスルーとなる新たな方法論の開発が必要不可欠です。当研究室では,ブレイクスルーとして,図2のとおり,元素間相乗効果を基盤とする鉄反応場の活性化に取り組みます。
第一に,鉄単独では反応性や活性が低くても,空間的に大きく広がり柔軟な電子状態をとる高周期典型元素との複合化させることで,高い活性をもつ反応場を構築します。そのためには,鉄と高集積典型元素の個性をとことん見つめ直す必要があり,無機化学的なアプローチが有効です。
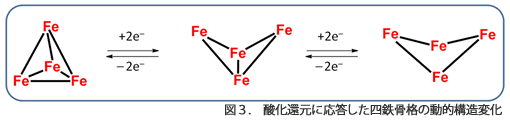
第二に,鉄そのものを複合化し,高活性化を図るアプローチも行っている。これはまさに,極めて高い触媒活性を示す,金属固体触媒と錯体触媒の中間に位置するもので,今後の発展が期待されます。当研究室では特に,四鉄骨格の酸化還元に応答した可逆的な動的挙動を報告し,世界をリードしています(図3)。このような特性を踏まえて,四鉄上での二酸化炭素など不活性炭素資源の資源化にも取り組んでいます。